热力学循环
简介
热力学循环是一系列传递热量并做功的热力学过程组成的集合,通过压强、温度等状态变量的变化,最终使热力学系统回到初始状态。状态量只依赖于热力学状态,沿热力学循环路径对此类物理量的路径积分结果为零;而像热量和功这样的过程量与循环过程有关,路径积分不为零。热力学第一定律指出在一个循环中输入的净热量总等于输出的净功。过程可重复的特性使得系统能够被连续操作,从而热力学循环是热力学中一个很重要的概念。在实际应用中,热力学循环经常被看作是一个准静态过程并被当作实际热机和热泵的工作模型。
P-V图
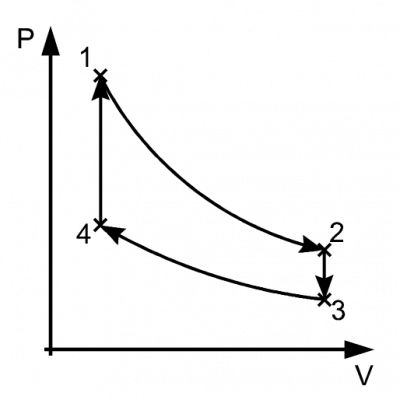
一个热力学循环(斯特灵循环)的P-V图
在P-V图上热力学循环可表示为一个闭合曲线,P-V图的Y轴表示压强,X轴表示体积,则闭合曲线所包围的面积等于过程所做的功$ \displaystyle W\, $:
$ \displaystyle {\text{(1)}}\qquad W=\oint P\ dV $.
这个功在数值上等于传入系统的热量$ \displaystyle Q\, $:
$ \displaystyle {\text{(2)}}\qquad W=Q=Q_{in}-Q_{out} $.
方程(2)的表达式显示热力学循环类似于一个等温过程,不过在循环过程中系统的内能是变化的,只是当每一次循环结束时系统内能会回到初始值。
如果循环过程在P-V图上是沿顺时针方向进行的,这个循环代表着一个热机,此时的输出功是正值;如果是沿逆时针方向进行的,则它代表这一个热泵,此时的输出功是负值。
热力学循环的类型
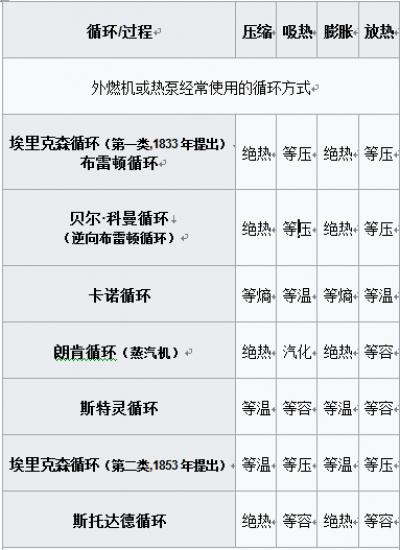
理论上一个热力学循环由三个或多个热力学过程组成(通常为四个),这些过程可以为:
- 等温过程 (温度恒定,即使伴随有吸热或放热过程)
- 等压过程 (压强恒定)
- 等容过程 (体积恒定)
- 绝热过程 (系统与外界无热交换)
- 等熵过程(可逆绝热过程) (系统与外界无热交换,同时熵保持恒定)
- 等焓过程 (焓保持恒定)
参考文献
- Halliday, Resnick & Walker. Fundamentals of Physics, 5th edition. John Wiley & Sons, 1997. Chapter 21, Entropy and the Second Law of Thermodynamics.
- Walter Greiner; Ludwig Neise, Horst Stöcker. Thermodynamics and Statistical Mechanics. Springer. 2008-05-23. ISBN 978-0387942995 (英语).


评论